Semaglutid in Deutschland — rechtlicher Rahmen und Bezugswege (nur Apotheke)
Semaglutid ist verschreibungspflichtig. Dieser Artikel erklärt den rechtlichen Rahmen, die legalen Bezugswege und die Gefahren nicht autorisierter Quellen.
Rechtlicher Hinweis (zwingend)
Semaglutid ist in Deutschland ein verschreibungspflichtiges Arzneimittel (AMG § 48). Der legale Bezug erfolgt ausschließlich auf ärztliche Verschreibung über eine deutsche Apotheke. Dieser Artikel ist keine Anleitung zum Graumarktkauf und keine Bezugsquelle. Werbung für verschreibungspflichtige Arzneimittel außerhalb der Fachkreise ist nach HWG § 10 unzulässig. Unerlaubter Vertrieb erfüllt den Straftatbestand AMG § 95. Rechtsgrundlage zusätzlich: Art. L.5111-1 CSP.
Wirkstoff & Fertigarzneimittel
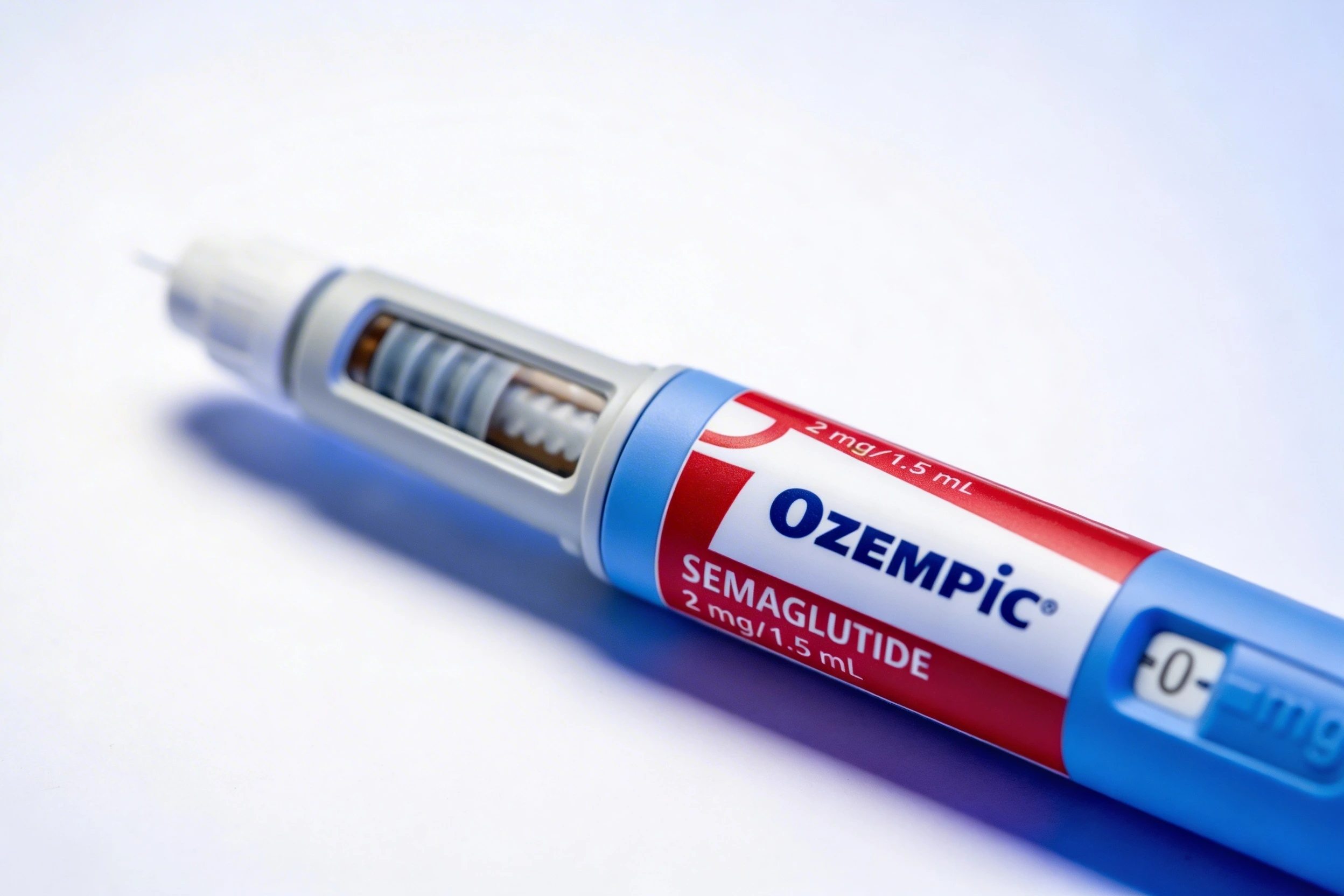
Semaglutid ist ein synthetisches GLP-1-Rezeptor-Agonist-Peptid von Novo Nordisk. Es ist in folgenden Fertigarzneimitteln enthalten:
- Ozempic® — s.c. Injektion, Indikation Typ-2-Diabetes mellitus (EMA 2018).
- Wegovy® — s.c. Injektion, Indikation Adipositas (EMA 2022).
- Rybelsus® — orale Formulierung, Typ-2-Diabetes (EMA 2020).
Alle drei Produkte sind verschreibungspflichtig.
Legaler Bezugsweg
- Konsultation bei einem niedergelassenen Arzt (Hausarzt, Diabetologe, Endokrinologe, Adipositas-Zentrum).
- Indikationsprüfung nach Fachinformation (BMI, Komorbiditäten, Kontraindikationen).
- Ausstellung eines Kassenrezepts oder Privatrezepts.
- Einlösung in einer deutschen Apotheke (vor Ort oder Versandapotheke mit Versanderlaubnis).
Krankenkassen erstatten Wegovy® in Deutschland nicht; Ozempic® wird bei Typ-2-Diabetes unter Beachtung der Wirtschaftlichkeitsregeln erstattet.
Gefahren nicht autorisierter Bezugsquellen
Online-Quellen, die Semaglutid ohne Rezept anbieten, operieren außerhalb des deutschen Arzneimittelrechts. BfArM und EMA haben mehrfach vor solchen Angeboten gewarnt:
- Fälschungen — Unterdosierung, falscher Wirkstoff, kontaminierte Zubereitungen.
- Keine Qualitätskontrolle nach Pharmakopöe-Standards.
- Keine Pharmakovigilanz — keine Erfassung von Nebenwirkungen.
- Strafbarkeit — Erwerb und Inverkehrbringen ohne Zulassung nach AMG § 95.
Abgrenzung Forschungsreagenz
Peptid-Anbieter führen gelegentlich „Semaglutid RUO" (research use only) als Laborreagenz. Diese Produkte sind keine Arzneimittel, entsprechen nicht den Pharmakopöe-Standards und dürfen nicht am Menschen angewendet werden. Sie dienen ausschließlich In-vitro-Studien in der wissenschaftlichen Forschung.
Lieferengpässe und Pharmakovigilanz
BfArM meldet wiederholt Lieferengpässe bei Semaglutid-Arzneimitteln infolge hoher Nachfrage. Aktuelle Lieferstatus sind auf bfarm.de einsehbar. Patientinnen und Patienten sollten Verdachtsfälle von Nebenwirkungen an nebenwirkungen.bund.de melden.
Rechtlicher Hinweis
Dieser Artikel dient der wissenschaftlich-rechtlichen Information. Er ersetzt keine ärztliche Beratung und enthält keine Bezugsquellen. Alle Informationen stehen unter dem Vorbehalt der aktuellen Fachinformation und BfArM-Rote-Hand-Briefe.
Forschungspeptide bestellen
Reinheit >99 %. Sichere Zahlung per Karte, Apple Pay oder Google Pay. Diskreter Versand europaweit.
Verwandte Artikel
Ozempic in Deutschland — Wissenschaftliche Information zu Semaglutid (Research Context)
Neutrale wissenschaftliche Einordnung von Semaglutid (Handelsname Ozempic®): Molekül, Rezeptor, Studiendaten und rechtlicher Status in Deutschland. Keine Kaufempfehlung.
Recht & QualitätTirzepatid (Mounjaro®) in Deutschland — rechtlicher Rahmen und Bezugswege
Tirzepatid ist verschreibungspflichtig. Wissenschaftlich-rechtliche Einordnung von Mounjaro® und Zepbound® in Deutschland.
ForschungSemaglutid — Studiendosierungen aus Ozempic® / Wegovy® Zulassungsstudien
Welche Dosierungen wurden in den Zulassungsstudien von Semaglutid geprüft? Wissenschaftliche Zusammenfassung, keine Humanempfehlung.
ForschungTirzepatid — Studiendosierungen aus SURPASS / SURMOUNT (Mounjaro® Fachinformation)
Welche Dosierungen wurden in den Zulassungsstudien von Tirzepatid geprüft? Wissenschaftliche Zusammenfassung, keine Empfehlung zur Humananwendung.
